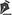RESUMO
Objetivo: Destacar a importância do tromboembolismo venoso como fator de morbidade e mortalidade em pacientes queimados. Relato de caso: Paciente do sexo masculino, 27 anos, vítima de queimadura por corrente elétrica e chama, com comprometimento de 19% de superfície corporal queimada. Apresentou, após 5ª semana de internaçao, trombose de veia profunda de membro inferior e embolia pulmonar nao fatal. Conclusao: Além dos fatores comuns a outros grupos, os pacientes queimados apresentam-se expostos a outros fatores de risco para tromboembolismo pulmonar, com destaque para queimadura de extremidades, infecçao de áreas queimadas e deficiência de antitrombina III. A sistematizaçao do tratamento de pacientes queimados deve incluir a profilaxia antitrombótica e a rápida implementaçao do tratamento específico para o tromboembolismo.
Palavras-chave:
Queimaduras. Trombose venosa. Embolia pulmonar.
ABSTRACT
Aim: To detach the thromboembolism's importance as a factor of morbility and mortality in burned patients. Case report: Twenty-seven years old male patient, burn victim by eletricity and fire, with 19% of the total body surface area. The patient presented, after 5th week of hospitalization, deep vein thrombosis and non-fatal pulmonary embolism. Conclusion: Besides the common factor to others groups, burned patients are exposed to others risk factors to pulmonary thromboembolism, with eminence for burned extremities, burned area infection and antithrombin III deficiency. The treatment's systematization must include the antithrombotic prophylaxis and quickly use of especific therapy to pulmonary thromboembolism.
Keywords:
Burns. Venous thrombosis. Pulmonary embolism..
O embolismo pulmonar provoca manifestaçoes clínicas que variam desde um quadro assintomático até a morte súbita. A natureza dessa obstruçao intravascular pode ser endógena (trombo, líquido amniótico, células tumorais, êmbolos sépticos ou gordura) ou exógena (talco de luvas de pacientes usuários de drogas injetáveis)1,2.
O local de origem mais comum de êmbolos para a circulaçao pulmonar é o sistema venoso profundo dos membros inferiores1-4. Naqueles em que o local de origem do embolo é descoberta, 70-90% dos pacientes apresentam um ou mais trombos na regiao íleo-femoral do sistema venoso profundo dos membros inferiores4, com um número crescente de casos originando-se de veias pélvicas4. A correlaçao entre a localizaçao do trombo e a incidência e gravidade da embolia pulmonar foi demonstrada em um estudo retrospectivo4, no qual a incidência de embolia pulmonar quando os trombos se localizaram na panturrilha, coxa e veias pélvicas foi de 46%, 67% e 77%, respectivamente. Enquanto a origem cardíaca de êmbolos corresponde a uma pequena fraçao na incidência global de embolismo pulmonar4,5, há relatos de aumento na incidência por êmbolos originários de veias dos membros superiores, possivelmente pela realizaçao de procedimentos diagnósticos e terapêuticos4.
A embolia pulmonar é responsável direta por aproximadamente 50.000 mortes anualmente nos Estados Unidos5. A incidência de tromboembolismo venoso é de 7 a 10 por 10.000 habitantes5-7, metade dos casos ocorrendo em pacientes hospitalizados7. Dentro do subgrupo de pacientes queimados, encontramos a incidência de trombose venosa profunda e embolia pulmonar entre 0,25 a 23% e 0 a 2,9%, respectivamente8-11. No entanto, estudos de autopsias em pacientes queimados já demonstraram incidência de embolismo pulmonar tao alta quanto 30%11.
A taxa de mortalidade da embolia pulmonar encontra-se em 6-15%4,7,8, podendo chegar a 30% nos pacientes nao tratados7. A embolia pulmonar ainda é responsável por uma alta taxa de mortalidade nos meses seguintes à sua ocorrência4.
RELATO DO CASO Paciente do sexo masculino, com 27 anos, foi vítima de queimadura por eletricidade e chama (arco voltaico), em ambiente de trabalho, com comprometimento de períneo e membros inferiores, totalizando 19% de superfície corporal queimada, segundo diagrama de Lund-Browder. Associado à queimadura, houve politraumatismo em decorrência de queda de 8 metros aproximadamente, com fraturas de 5ª e 8ª costelas direitas (Figura 1), fraturas de processos transversos de L
1 a L
4 (Figura 2) e hematoma em músculo pssoas em regiao lombar, diagnosticados por tomografia computadorizada realizada no momento da internaçao. Houve relato de perda de consciência no local do trauma por tempo indeterminado. Paciente foi internado hemodinamicamente estável.
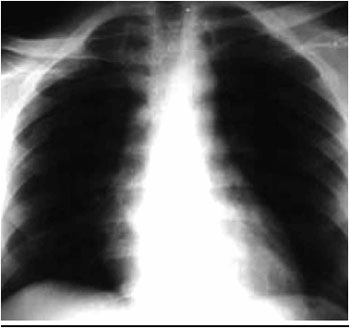
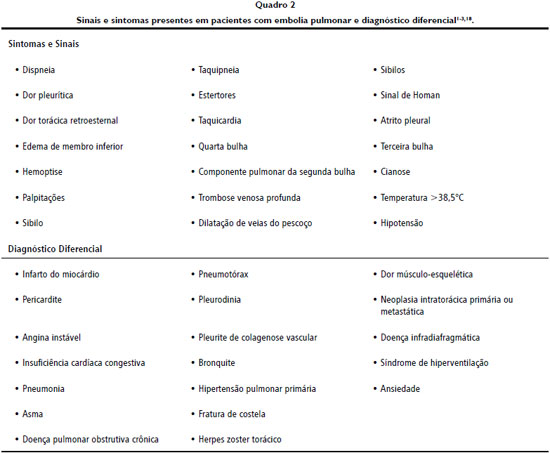
Figura 1 - Fraturas de costelas direitas.
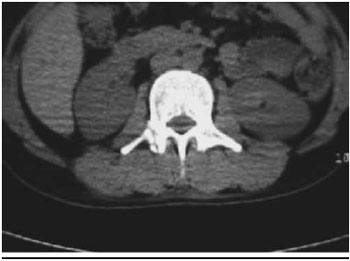
Figura 2 - Fratura de processo transverso de vértebra lombar.
Glasgow 15/15, diurese presente, recebendo hidrataçao e analgesia venosa. Refere história prévia de angina aos grandes esforços, com melhora após repouso. Eletrocardiograma realizado à admissao nao revelou nenhuma alteraçao. Iniciou-se profilaxia para trombose venosa profunda (TVP) com heparina de baixo peso molecular (HBPM), enoxiparina, no segundo dia de internaçao. No quarto dia, em decorrência da presença de picos febris, foi administrada antibioticoterapia venosa com oxacilina e amicacina, após a obtençao de hemocultura e fragmento de pele por biopsia. Ambas positivaram-se para
Klebisiela pneumonia, sensível a imipenem, meropenem e amicacina. Associou-se imipenem ao esquema, o qual foi suspenso após a primeira dose devido à reaçao urticariforme, tratada com corticoterapia venosa. O esquema antibiótico acima citado permaneceu por 14 dias. Na terceira semana de internaçao, desenvolveu flebite superficial em membro superior direito, tratada com cefalosporina venosa por 10 dias.
A profilaxia da TVP foi suspensa após uma semana de deambulaçao pelo paciente, no 28° dia de internaçao. Uma semana após a suspensao da profilaxia, o paciente apresentou edema em membro inferior esquerdo, associado a dor local e sinal de Homan positivo. Iniciou-se HBPM em dose terapêutica. Após três dias de terapia anticoagulante, paciente manifestou dor torácica, tipo pleurítica, e taquipnéia. Encontrava-se hemodinamicamente estável. A dose de HBPM foi aumentada e a tomografia computadorizada com contraste venoso realizada mostrou derrame pleural à esquerda, com atelectasia adjacente; consolidaçao associada a vidro fosco adjacente na periferia do segmento anterior do lobo superior esquerdo; e falha de enchimento na extremidade da artéria pulmonar esquerda e no ramo segmentar inferior deste lado (Figura 3), sugestivo de trombose. Associou-se o anticoagulante oral varfarina e o paciente recebeu alta hospitalar após duas semanas com INR dentro da faixa desejável (2-3).
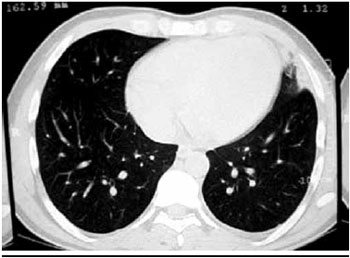
Figura 3 - Tomografia computadorizada com área de infarto pulmonar.
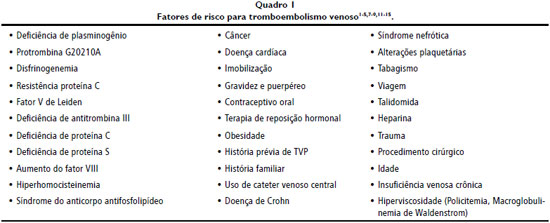
A cascata de coagulaçao é um mecanismo fisiológico de controle da perda sanguínea por meio do equilíbrio entre componentes endoteliais, plaquetas e proteínas plasmáticas5. Como descrito por Virchow, a estase venosa, o dano vascular e a hipercoagulabilidade sao fatores trombogênicos. O organismo possui mecanismos de oposiçao à trombogênese, dentre os quais incluímos os inibidores circulantes (antitrombina III, α2-macroglobulina, α1-antitripsina, proteína C ativada), clearance de fatores de coagulaçao e complexos de polímero de fibrina pelo sistema retículo endotelial e fígado, enzimas fibrinolíticas derivadas do endotélio e células plasmáticas e a açao leucocitária2. Em algumas situaçoes (Quadro 1), ocorre a ativaçao da cascata de coagulaçao de forma inadequada e descontrolada, sobrepujando os sistemas antitrombóticos, trazendo consequências deletérias ao organismo, na forma de eventos trombóticos arteriais e venosos.
Os pacientes queimados parecem apresentar alto risco de desenvolver tromboembolismo pulmonar devido a imobilizaçao, repetidos procedimentos cirúrgicos e uso de cateteres centrais8,11. Estudos têm destacado a importância da sepse e da queimadura em extremidades como fatores de risco8,15 e da deficiência de antitrombina III na fisiopatologia do tromboembolismo venoso nos pacientes queimados7,11,15,16. O estado de hipercoagulabilidade plasmática no paciente queimado pode começar após 2 a 3 horas da queimadura, devido à ativaçao da cascata de coagulaçao pela exposiçao direta do colágeno17.
Dois fatores sao cruciais na determinaçao da sintomatologia da embolia pulmonar e definiçao de seu desfecho, sao eles a magnitude da embolizaçao e a pré-existência de doença cardíaca e/ou pulmonar4.
Com a obstruçao do fluxo da artéria pulmonar, ocorre aumento da pressao no ventrículo direito, com consequentes aumentos do trabalho miocárdico e do consumo de oxigênio. A deterioraçao miocárdica é explicada pela diminuiçao do gradiente pressórico entre aorta e ventrículo direito, dilataçao do ventrículo direito e abaulamento do septo interventricular em direçao à câmara do ventrículo esquerdo3,4.
No pulmao, havendo obstruçao completa da luz do vaso sanguíneo, observa-se aumento da resistência vascular e das vias aéreas, comprometimento da troca gasosa devido ao aumento do espaço morto alveolar, diminuiçao do surfactante, áreas de atelectasia e hiperventilaçao alveolar1-4.
Ambos os pulmoes sao acometidos, principalmente os lobos inferiores. O infarto, caracterizado histologicamente por hemorragia intra-alveolar e destruiçao das paredes dos alvéolos, é uma exceçao, devido à existência de dupla vascularizaçao pulmonar, sendo mais comum em áreas periféricas, supridas por artérias de pequeno calibre. O infarto pulmonar ocorre principalmente em pacientes com doenças cardíacas ou pulmonares pré-existentes 4.
No Quadro 2, encontramos os principais sinais e sintomas presentes em pacientes com embolia pulmonar e as doenças com as quais deve-se realizar diagnóstico diferencial.
Dentro dos métodos diagnósticos, a arteriografia é o "padrao ouro", definindo a embolia pulmonar quando observa um defeito de enchimento intraluminal em mais de uma incidência. Sinais secundários incluem a interrupçao abrupta dos vasos, oligoemia segmentar ou ausência de vascularizaçao, fase arterial prolongada com enchimento lento ou vasos periféricos tortuosos e progressivamente menores. A arteriografia apresentou em um estudo morbidade e mortalidade de 1% e 0,5%, respectivamente18.
Destacam-se, ainda, a dosagem do D-dímero, cintilografia ventilaçao-perfusao e a tomografia computadorizada helicoidal. A dosagem do D-dímero, produto da degradaçao da fibrina pela plasmina, pelo método Elisa, demonstra alta sensibilidade para embolismo pulmonar, mas baixa especificidade, por apresentar níveis aumentados também em pacientes hospitalizados, grávidas7, doenças vasculares periféricas, câncer, doenças inflamatórias e idade avançada4. A cintilografia de ventilaçao-perfusao mostra a discordância entre áreas ventiladas e nao perfundidas em exames com alta probabilidade de embolismo pulmonar, porém é importante salientar que o estudo PIOPED18 demonstrou embolismo pulmonar diagnosticado por arteriografia em 12% dos pacientes com uma cintilografia de baixa probabilidade e em 33% com probabilidade intermediária.18,19. A tomografia computadorizada helicoidal vem substituindo a cintilografia em vários centros2,7,20. Apresenta alta sensibilidade e especificidade para êmbolos localizados nas artérias pulmonares principais, lobares e segmentares, com decréscimo para os êmbolos localizados na periferia pulmonar4,7, no entanto, estes nao parecem ter grande importância clínica19. A tomografia computadorizada helicoidal consegue excluir outros diagnósticos e fornecer informaçoes sobre o prognóstico do paciente19,21.
No eletrocardiograma, as alteraçoes em seus diversos segmentos e as manifestaçoes de
cor pulmonale, presente em apenas uma fraçao dos pacientes com embolismo pulmonar, sao inespecíficas, porém é útil na exclusao de outras patologias1-3,19,21. Os níveis de troponina7, marcador de lesao miocárdica, podem estar elevados principalmente nas embolias maciças, porém nao possuem sensibilidade suficiente para serem usados como método diagnóstico1-3 ou como fator determinante de prognóstico21. A determinaçao do nível de PaO
2 pela gasometria nao tem utilidade diagnóstica2,4,18. Frequentemente a radiografia de tórax é anormal, porém derrame pleural, atelectasia, elevaçao discreta do hemidiafragma, entre outros, sao inespecíficos e os sinais clássicos de infarto (giba de Hampton e sinal de Westermark) sao infrequentes. A ressonância nuclear magnética tem baixa sensibilidade para êmbolos nas artérias subsegmentares7, porém tem utilidade no diagnóstico da trombose venosa profunda de membros inferiores, assim como a ultrassonografia com Doppler, sendo um subsídio para o diagnóstico de embolia pulmonar. O ecocardiograma pode identificar anomalias do ventrículo direito, corroborando o diagnóstico de embolia pulmonar4,7, além de identificar pacientes que se beneficiariam da terapia trombolítica ou aqueles com maiores chances de desenvolverem complicaçoes nos meses subsequentes2,21.
O tratamento de suporte com ventilaçao mecânica, uso de vasopressores, entre outras medidas, deve ser sempre aplicado quando necessário. Incluímos entre as opçoes de tratamento da embolia pulmonar o uso de anticoagulantes, agentes fibrinolíticos, a inserçao de filtros na veia cava e a embolectomia cirúrgica.
A anticoagulaçao é a pedra fundamental no tratamento da embolia pulmonar. Sem a adequada anticoagulaçao, até 50% dos pacientes podem apresentar recorrência de tromboembolismo venoso nos três primeiros meses16, sofrendo uma queda desse índice para 10% em 2 anos, quando ocorre anticoagulaçao de forma satisfatória2.
A heparina nao fracionada (HnF), por meio da sua açao sobre a antitrombina III, é eficaz no tratamento da embolia pulmonar2,4,7, com diminuiçao da mortalidade. Ela é acompanhada pelo tempo de tromboplastina parcial ativada, estando o valor desejável entre 1,5 e 2,0 do tempo controle. As principais complicaçoes sao hemorragia, trombocitopenia e osteoporose. O argatroban e a lepirudina podem ser usados no tromboembolismo venoso com trombocitopenia induzida pela heparina2. A HBPM apresenta maior biodisponibilidade e maior poder de inibiçao do fator Xa. O uso de HBPM mostrou-se tao eficaz e seguro quanto a HnF, com menor risco de trombocitopenia2, com diminuiçao na mortalidade da embolia pulmonar2-4,6,7. A hirudina e outros inibidores diretos da trombina possuem uma eficácia maior que a heparina, porém apresentam maior risco de sangramento1,2. Novos anticoagulantes estao sendo desenvolvidos, sem as limitaçoes de seus predecessores e com eficácia semelhante ou maior2,19.
A varfarina, anticoagulante oral, impede a ativaçao por γ-carboxilaçao dos fatores II, VII, IX e X, e também das proteínas C e S, criando um ambiente trombogênico paradoxal. Portanto, deve ser sempre utilizada associada com a heparina por um breve período de tempo. Tem como maiores complicaçoes a hemorragia, necrose cutânea relacionada com a queda dos níveis de proteína C e o potencial de má formaçao fetal, principalmente quando usada entre a sexta e décima segunda semana de gestaçao1-4.
Os agentes trombolíticos ativam o plasminogênio, produzindo plasmina. Sao utilizados em pacientes com instabilidade hemodinâmica ou oxigenaçao gravemente comprometida, comprometimento embólico correspondente à metade do leito vascular pulmonar, trombose venosa profunda extensa acompanhada de embolia submaciça e disfunçao ventricular direita, sem hipotensao ou hipoxemia grave2,19. As contraindicaçoes ao seu uso incluem sangramento interno ativo, hemorragia cerebral, trauma cerebral ou medular recente, neoplasia intracraniana, má formaçao arteriovenosa, hipertensao importante nao controlada e episódio de diátese hemorrágica1-4,19,21. Sua principal complicaçao é a hemorragia, inclusive intracraniana4,7,19,21.
A interrupçao da veia cava por posicionamento de filtro é utilizada naqueles pacientes com contraindicaçao à anticoagulaçao, em embolia recente em vigência de tratamento anticoagulante adequado e em casos com complicaçoes hemorrágicas graves durante o tratamento anticoagulante.
A embolectomia cirúrgica é reservada para pacientes hemodinamicamente instáveis ou chocados, aqueles que possuem contraindicaçao para o emprego de anticoagulaçao ou que nao respondem à terapia trombolítica 6,7,21.
DISCUSSAO Embora os pacientes queimados preencham os critérios da tríade de Virchow, além da coexistência de diversos fatores de risco, eles apresentam incidência de tromboembolismo pulmonar clinicamente significativa menor do que seria esperado. A verdadeira incidência de eventos tromboembolicos nos pacientes queimados ainda nao é conhecida. Os dados apresentados pelos diversos estudos baseiam-se, em grande parte, em trabalhos retrospectivos através da análise dos prontuários daqueles pacientes que apresentaram quadro clínico compatível com eventos tromboembólicos. Nos estudos prospectivos, a populaçao de pacientes queimados, apesar de terem significância estatística, é pequena. Por esses dois fatos, pode-se presumir que um grande número de casos de tromboembolismo venoso nao é diagnosticado, o que é corroborado pela alta incidência de eventos tromboembólicos descobertos em estudos de autopsias, apesar desses terem sido realizados em uma época na qual possivelmente nao se usava a terapia anticoagulante e outros métodos profiláticos, como atualmente.
Dentre os fatores de risco, temos uma maior importância da presença de queimadura nas extremidades inferiores, a ocorrência de infecçao e a deficiência de antitrombina III. Destacam-se, ainda, o grande período de imobilizaçao, o uso de cateteres venosos profundos e os diversos procedimentos cirúrgicos aos quais os pacientes queimados sao submetidos.
Na terapia anticoagulante se fundamenta o tratamento do tromboembolismo pulmonar, permanecendo as outras modalidades terapêuticas como opçoes naqueles que se apresentam hemodinamicamente instáveis ou com complicaçoes e/ou contraindicaçoes ao uso dos anticoagulantes. O uso da heparina de baixo peso molecular mostrou-se segura e com menor índice de complicaçoes quando comparada à HnF.
Os pacientes com tromboembolismo pulmonar apresentam risco de embolia pulmonar recorrente e taxa de mortalidade4 maiores quando comparados àqueles que só apresentaram trombose venosa profunda. Esse aumento da mortalidade pode decorrer de doenças concomitantes ou de novos episódios de embolia pulmonar.
Com a anticoagulaçao adequada, a incidência de embolia pulmonar recorrente, fatal ou nao, é reduzida para menos de 8%7.
CONCLUSAO Os pacientes queimados apresentam condiçoes propícias ao aparecimento de eventos tromboembólicos devido à coexistência de diversos fatores de risco. A melhor forma de tratar o tromboembolismo venoso é estabelecer uma sistematizaçao do atendimento ao paciente queimado com a implementaçao de uma rotina com profilaxia anticoagulante, utilizaçao de mecanismos de compressao pneumática intermitente, quando possível, diminuiçao do tempo de imobilizaçao no leito e uso racional de cateteres venosos profundos. Naqueles com embolia pulmonar, a terapia anticoagulante e os outros métodos devem ser iniciados com rapidez, a fim de se preservar a vida do paciente. Após alta hospitalar, o paciente deve ser acompanhado devido à possibilidade de episódios recorrentes, principalmente no primeiro ano.
REFERENCIAS1. Mc Phee SJ, Papadakis MA. Current medical diagnosis & treatment. 48
th ed. New York:McGraw-Hill;2009.
2. Goldman L, Ausiello D. Tratado de medicina interna. 22ª ed. Rio de Janeiro: Guanabara Koogan;2005. p.646-54.
3. Fauci AS, Braunwald E, Kasper DL, Hauser SL, Longo DL, Jameson JL, et al. Harrison's principles of internal medicine. 17th ed. New York:McGraw Hill;2008.
4. Torbicki A, van Beek EJR, Charbonnier B, Meyer G, Morpurgo M, Palla A, et al. Guidelines on diagnosis and management of acute pulmonary embolism. Task Force Report on Pulmonary Embolism, European Society of Cardiology. Eur Heart J. 2000; 21(16):1301-36.
5. Dutta TK, Venugopal V. Venous thromboembolism: the intricacies. J Postgrad Med. 2009;55(1):55-64.
6. Segal JB, Streiff MB, Hofmann LV, Thornton K, Bass EB. Management of venous thromboembolism: a systematic review for a practice guideline. Ann Intern Med. 2007;146(3):211-22.
7. British Thoracic Society Standards of Care Committee Pulmonary Embolism Guideline Development Group. British Thoracic Society guidelines for the management of suspected acute pulmonary embolism. Thorax. 2003;58(6):470-83.
8. Wahl WL, Brandt MM, Ahrns KS, Zajkowski PJ, Proctor MC, Wakefield TW, et al. Venous thrombosis incidence in burn patients preliminary results of a prospective study. J Burn Care Rehabil. 2002;23(2):97-102.
9. Ferguson RE, Critchfield A, Leclaire A, Ajkay N, Vasconez HC. Current practice of thromboprophylaxis in the burn population: a survey study of 84 US burn centers. Burns. 2005;31(8):964-6.
10. Fecher AM, O'Mara MS, Goldfarb IW, Slater H, Garvin R, Birdas TJ, et al. Analysis of deep vein thrombosis in burn patients. Burns. 2004;30(6):591-3.
11. Barret JP, Dziewulski PG. Complications of the hypercoagulable status in burn injury. Burns. 2006;32(8):1005-8.
12. Masaki F, Isao T, Aya Y, Nakayama R, Tadaaki Y, Hideyosi T. Extensive thrombosis of the inferior vena cava and portal vein following electrical injury. Burns. 2005;31(5):660-4.
13. Germann G, Kania NM. Extensive thrombosis of the caval venous system after central venous catheters in severely burned patients. Bums. 1995;21(5):389-91.
14. Niedermayr M, Schramm W, Kamolz L, Andel D, Romer W, Hoerauf K, et al. Antithrombin deficiency and its relationship to severe burns. Burns. 2007;33(2):173-8.
15. Garcia Torres V, Jimenez MC, Garcia Salvatierra B, Rivera MJ, Guemes Gordo F. Modifications of coagulation in the burn patient. Ann MBC. 1991;4(1):16.
16. Chapman NH, Brighton T, Harris MF, Caplan GA, Braithwaite J, Chong BH. Venous thromboembolism: management in general practice. Aust Fam Physician. 2009;38(1-2):36-40.
17. Lima Junior EM, Novaes FN, Piccolo NS, Valle MC. Tratado de queimaduras no paciente agudo. 2ª ed. Rio de Janeiro:Atheneu.
18. Stein PD, Terrin ML, Hales CA, Palevsky HI, Saltzman HA, Thompson BT, et al. Clinical, laboratory, roentgenographic, and electrocardiographic findings in patients with acute pulmonary embolism and no pre-existing cardiac or pulmonary disease. Chest. 1991;100(3):598-603.
19. Lee CH, Hankey GJ, Ho WK, Eikelboom JW. Venous thromboembolism: diagnosis and management of pulmonary embolism. Med J Aust. 2005;182(11):569-74.
20. Perrier A, Howarth N, Didier D, Loubeyre P, Unger PF, de Moerloose P, et al: Performance of helical computed tomography in unselected outpatients with suspected pulmonary embolism. Ann Intern Med. 2001;135(2):88-97.
21. Carlbom DJ, Davidson BL. Pulmonary embolism in the critically ill. Chest. 2007;132(1):313-24.
1. Cirurgiao Plástico do Centro de Tratamento de Queimado - Hospital do Andaraí; Membro Especialista da Sociedade Brasileira de Cirurgia Plástica; Membro da Sociedade Brasileira de Queimaduras.
2. Pós-graduanda em Dermatologia, Hospital Universitário Pedro Ernesto.
3. Chefe do Centro de Tratamento de Queimado (CTQ) do Hospital Federal do Andaraí.
4. Chefe do Centro de Tratamento de Queimado Adulto (CTQ-A) do Hospital Municipal Souza Aguiar - Rio de Janeiro. Coordenadora Clínica do Centro de Tratamento de Queimado (CTQ) do Hospital Federal do Andaraí - Rio de Janeiro. Professora do Internato (Módulo Queimaduras) da Universidade Gama Filho, Instrutora do Curso Nacional de Normatizaçao ao Atendimento do Queimado (CNNAQ) da SBQ e Curso ABIQ da FELAQ.
Correspondência:
Flávio Lima Magalhaes
Rua Engenheiro Enaldo Cravo Peixoto, 65 / 1105 - Tijuca
Rio de Janeiro, RJ - CEP 20511-230
E-mail: flaviolimamagalhaes@globo.com
Recebido em: 3/2/2010
Aceito em: 22/4/2010
Trabalho realizado no Centro de Tratamento de Queimados - Hospital do Andaraí, Rio de Janeiro, RJ.